شخصی سازی درمان سیستیک فیبروزیس
بیماری سیستیک فیبروزیس یک بیماری مزمن پیشرونده است. این بیماری در اثر جهش در ژن تنظیم کننده انتقال دهنده غشایی کلر (cystic fibrosis transmembrane conductance regulator (CFTR)) ایجاد می شود و بصورت اتوزومال مغلوب به ارث می رسد. به دلیل تنوع ژنتیکی بالا در مبتلایان به این بیماری و نبود یک مدل آزمایشگاهی مناسب، یافتن روش درمانی بهینه بصورت کامل محقق نشده بود.
علائم بیماری سی اف چیست؟
سی اف بهعنوان مهمترین عامل بیماری مزمن ریوی در کودکان بوده و عامل اکثر موارد نارسایی لوزالمعده در اوایل زندگی می باشد. سی اف عامل بسیاری از موارد از دست دادن نمک، پولیپهای بینی، سینوزیت تمام سینوس ها، بیرون زدگی راست روده، دیابت، نارسایی رشد و اختلالات کبدی می باشد.
علائم این بیماری:
۱.بوسه شور و عرق فراوان و شوره زدن لباسها
۲. سرفه مزمن که به روش های درمان معمول بهبود نیافته و در اوائل بیماری خشک ولی در نهایت خلطی می شود
۳. عفونتهای مکرر ریوی
۴. خس خس و تنگی نفس
۵. عدم وزن گیری علی رغم اشتهای خوب بیمار
۶. دفع مکرر مدفوع چرب و گریس مانند با حجم زیاد
۷. نازائی
علت ایجاد بیماری:
سیستیک فیبروزیس زمانی اتفاق میافتد که پروتئین تنظیمکننده کانال غشایی انتقال دهنده کلر دچار مشکل شود.
پروتئین تنظیم کننده کانال غشایی انتقال دهنده کلر به حفظ تعادل نمک و آب در بسیاری از سطوح بدن مانند سطح ریه کمک می کند. این کانال نوع خاصی از پروتئین است که کانال یونی نامیده می شود و در ریه، این کانال یونی، یون های کلرید را از داخل سلول به خارج از سلول منتقل می کند.
برای درک اینکه چگونه جهش در ژن کانال غشایی انتقال دهنده کلر باعث اختلال در عملکرد پروتئین می شود، مهم است که بدانیم پروتئین به طور معمول چگونه ساخته می شود و چگونه به انتقال آب و کلرید به سطح سلول کمک می کند. پروتئین کانال غشایی انتقال دهنده کلر از 1480 اسید آمینه تشکیل شده است. هنگامی که زنجیره پروتئین کانال غشایی انتقال دهنده کلر ساخته شد، به شکل فضایی خاصی (Folding) در می آید.
هنگامی که یون های کلرید در خارج از سلول قرار می گیرند، لایه ای از آب را جذب می کنند. این لایه آب از این جهت مهم است که به موهای ریز روی سطح سلول های ریه که مژه نامیده می شوند اجازه می دهد تا به جلو و عقب بروند. این حرکت فراگیر موکوز را به سمت بالا و خارج از مجاری تنفسی حرکت می دهد.
هنگامی که کانال غشایی انتقال دهنده کلر به درستی کار نمی کند، کلرید - یکی از اجزای نمک - در سلول ها به دام می افتد. بدون حرکت مناسب کلرید، آب نمی تواند سطح سلولی را هیدراته کند. این امر باعث می شود که مخاط سطح سلول، ضخیم و چسبناک شود و بسیاری از علائم مرتبط با سیستیک فیبروزیس را ایجاد کند.
در افراد مبتلا به سیستیک فیبروزیس، جهش در ژن انتقال دهنده کانال کلر می تواند مشکلات زیر را در کانال پروتئینی انتقال دهنده کلر ایجاد کند: کانال های پروتئینی عملکرد صحیحی ندارند، به مقدار کافی تولید نمی شوند و یا اصلا تولید نمی شوند.
هنگامی که هر یک از این مشکلات رخ دهد، یون های کلرید در داخل سلول به دام می افتند و آب دیگر به فضای بیرون سلول جذب نمی شود. هنگامی که آب کمتری در خارج از سلول ها وجود دارد، مخاط موجود در راه های تنفسی غلیظ می شود و زمانی که مخاط غلیظ و چسبنده شود، مژه ها را سنگین می کنند و مژه ها نمی توانند به درستی زنش داشته باشند. در نتیجه مخاط در مجاری تنفسی گیر می کند و تنفس دچار مشکل خواهد شد. علاوه بر این میکروب های به دام افتاده در مخاط، دیگر از راه های تنفسی خارج نمی شوند و به آنها فرصت تکثیر و ایجاد عفونت داده می شود. مخاط غلیظ در ریه ها و عفونت های مکرر، از شایع ترین مشکلاتی است که افراد مبتلا به سیستسک فیبروزیس با آن ها مواجه هستند.
روش های درمانی:
با توجه به اینکه بیماری سیستیک فیروزیس بیشتر در کودکان شایع است و در صورت عدم درمان مناسب از طریق این دارو های مناسب، منجر به مرگ بیمار در سنین پایین می گردد، در نتیجه درمان این بیماری در زمان مناسب، اثرات اجتماعی، اقتصادی مثبتی در پی دارد. با ایجاد کردن این مدل ها و ارائه خدمات، کشور ما در بین محدود کشور های دست یافته به این تکنولوژی قرار می گیرد.
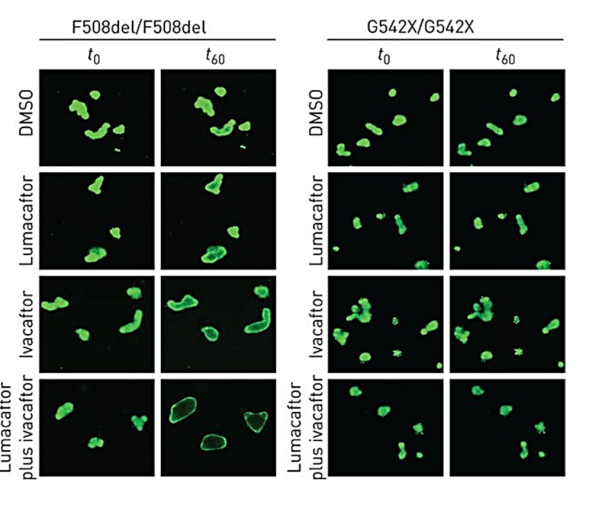
شرکت آمریکایی ورتکس (Vertex) در دهه اخیر میلادی، داروهایی که جهت درمان بیماران مبتلا به سیستیک فیبروزیس استفاده می شوند که شامل دارو های لوماکافتور و ایواکافتور و غیره است را از طریق مدل های ارگانوئیدی بافت منشاء گرفته از بیماران مبتلا به سیستیک فیروزیس آزمایش کرده و پس از اطمینان از پاسخدهی دارویی بر روی این مدل ها، تائیدیه FDA را دریافت کرد و دارو های خود را به بازار جهانی معرفی نمود.
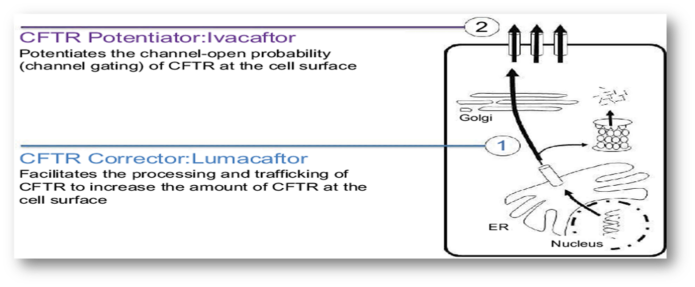
لوماکافتور(Lumacaftor): این دارو در جهت اصلاح مسیر انتقال پروتئین بیان شده توسط ژن کد کننده کانال غشایی انتقال دهنده کلر، از سیتوسل به سمت لایه خارجی غشاء پلاسمایی سلول عمل می کند. با استفاده از این دارو، شاهد افزایش حضور این پروتئین ها در اطراف غشاء پلاسمایی در سلول های افراد مبتلا به سیستیک فیبروزیس خواهیم بود.
ایواکافتور(Ivacaftor): این دارو در جهت باز نگه داشتن کانال غشایی انتقال دهنده کلر و افزایش عبور مواد از این کانال در غشاء پلاسمایی عمل می کند. با استفاده از این دو دارو، ما شاهد افزایش خروج یون کلراید از غشاء سلول و کاهش علائم این بیماران خواهیم بود.
شخصی سازی درمان بیماری سیتیک فیبروزیس:
شخصی سازی درمان شامل دو بخش می باشد. در بخش اول جهش های دخیل در کانال غشایی تنظیم کننده کلر (CFTR) از طریق بررسی های ژنتیکی مشخص می گردد. رایج ترین جهش F508 می باشد.
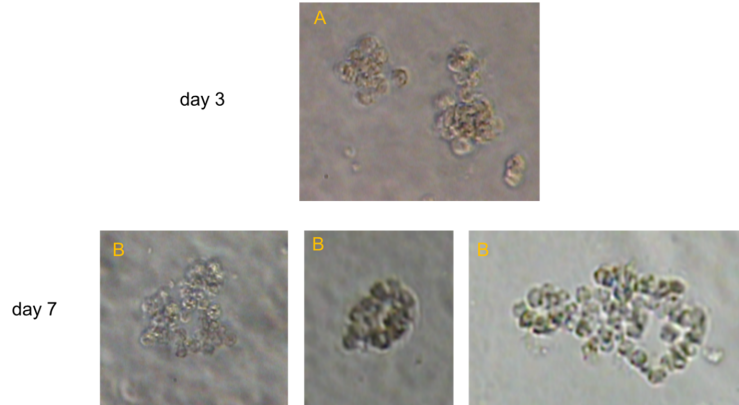
بخش دوم شامل مدل سازی ارگانوئیدی از بافت منشا گرفته از بیماران مبتلا به سیستیک فیبروزیس با جهش های دخیل در کانال غشایی تنظیم کننده کلر می باشد. پیشرفت در تکنولوژی مدل سازی ارگانوئیدی از بافت منشاء گرفته بیمار، این امکان را فراهم آورده است که بتوان با استفاده از نمونه بافت بیمار، درمان بیماران مبتلا به سیستیک فیبروزیس را شخصی سازی کرد. این مدل های برون تنی (In vitro)، به علت شباهت بسیار زیاد به لحاظ خصوصیات فیزیولوژیکی و ژنتیکی با بافت درون تنی بیمار (In vivo)، این قابلیت را فراهم آروده است که پاسخ دهی دارویی بر روی مدل های ارگانوئیدی بیمار، بطور دقیق منعکس کننده رفتار دارویی بر روی بافت بیمار باشد.
علائم بیماری سی اف چیست؟
سی اف بهعنوان مهمترین عامل بیماری مزمن ریوی در کودکان بوده و عامل اکثر موارد نارسایی لوزالمعده در اوایل زندگی می باشد. سی اف عامل بسیاری از موارد از دست دادن نمک، پولیپهای بینی، سینوزیت تمام سینوس ها، بیرون زدگی راست روده، دیابت، نارسایی رشد و اختلالات کبدی می باشد.
علائم این بیماری:
۱.بوسه شور و عرق فراوان و شوره زدن لباسها
۲. سرفه مزمن که به روش های درمان معمول بهبود نیافته و در اوائل بیماری خشک ولی در نهایت خلطی می شود
۳. عفونتهای مکرر ریوی
۴. خس خس و تنگی نفس
۵. عدم وزن گیری علی رغم اشتهای خوب بیمار
۶. دفع مکرر مدفوع چرب و گریس مانند با حجم زیاد
۷. نازائی
علت ایجاد بیماری:
سیستیک فیبروزیس زمانی اتفاق میافتد که پروتئین تنظیمکننده کانال غشایی انتقال دهنده کلر دچار مشکل شود.
پروتئین تنظیم کننده کانال غشایی انتقال دهنده کلر به حفظ تعادل نمک و آب در بسیاری از سطوح بدن مانند سطح ریه کمک می کند. این کانال نوع خاصی از پروتئین است که کانال یونی نامیده می شود و در ریه، این کانال یونی، یون های کلرید را از داخل سلول به خارج از سلول منتقل می کند.
برای درک اینکه چگونه جهش در ژن کانال غشایی انتقال دهنده کلر باعث اختلال در عملکرد پروتئین می شود، مهم است که بدانیم پروتئین به طور معمول چگونه ساخته می شود و چگونه به انتقال آب و کلرید به سطح سلول کمک می کند. پروتئین کانال غشایی انتقال دهنده کلر از 1480 اسید آمینه تشکیل شده است. هنگامی که زنجیره پروتئین کانال غشایی انتقال دهنده کلر ساخته شد، به شکل فضایی خاصی (Folding) در می آید.
هنگامی که یون های کلرید در خارج از سلول قرار می گیرند، لایه ای از آب را جذب می کنند. این لایه آب از این جهت مهم است که به موهای ریز روی سطح سلول های ریه که مژه نامیده می شوند اجازه می دهد تا به جلو و عقب بروند. این حرکت فراگیر موکوز را به سمت بالا و خارج از مجاری تنفسی حرکت می دهد.
هنگامی که کانال غشایی انتقال دهنده کلر به درستی کار نمی کند، کلرید - یکی از اجزای نمک - در سلول ها به دام می افتد. بدون حرکت مناسب کلرید، آب نمی تواند سطح سلولی را هیدراته کند. این امر باعث می شود که مخاط سطح سلول، ضخیم و چسبناک شود و بسیاری از علائم مرتبط با سیستیک فیبروزیس را ایجاد کند.
در افراد مبتلا به سیستیک فیبروزیس، جهش در ژن انتقال دهنده کانال کلر می تواند مشکلات زیر را در کانال پروتئینی انتقال دهنده کلر ایجاد کند: کانال های پروتئینی عملکرد صحیحی ندارند، به مقدار کافی تولید نمی شوند و یا اصلا تولید نمی شوند.
هنگامی که هر یک از این مشکلات رخ دهد، یون های کلرید در داخل سلول به دام می افتند و آب دیگر به فضای بیرون سلول جذب نمی شود. هنگامی که آب کمتری در خارج از سلول ها وجود دارد، مخاط موجود در راه های تنفسی غلیظ می شود و زمانی که مخاط غلیظ و چسبنده شود، مژه ها را سنگین می کنند و مژه ها نمی توانند به درستی زنش داشته باشند. در نتیجه مخاط در مجاری تنفسی گیر می کند و تنفس دچار مشکل خواهد شد. علاوه بر این میکروب های به دام افتاده در مخاط، دیگر از راه های تنفسی خارج نمی شوند و به آنها فرصت تکثیر و ایجاد عفونت داده می شود. مخاط غلیظ در ریه ها و عفونت های مکرر، از شایع ترین مشکلاتی است که افراد مبتلا به سیستسک فیبروزیس با آن ها مواجه هستند.
روش های درمانی:
با توجه به اینکه بیماری سیستیک فیروزیس بیشتر در کودکان شایع است و در صورت عدم درمان مناسب از طریق این دارو های مناسب، منجر به مرگ بیمار در سنین پایین می گردد، در نتیجه درمان این بیماری در زمان مناسب، اثرات اجتماعی، اقتصادی مثبتی در پی دارد. با ایجاد کردن این مدل ها و ارائه خدمات، کشور ما در بین محدود کشور های دست یافته به این تکنولوژی قرار می گیرد.
شرکت آمریکایی ورتکس (Vertex) در دهه اخیر میلادی، داروهایی که جهت درمان بیماران مبتلا به سیستیک فیبروزیس استفاده می شوند که شامل دارو های لوماکافتور و ایواکافتور و غیره است را از طریق مدل های ارگانوئیدی بافت منشاء گرفته از بیماران مبتلا به سیستیک فیروزیس آزمایش کرده و پس از اطمینان از پاسخدهی دارویی بر روی این مدل ها، تائیدیه FDA را دریافت کرد و دارو های خود را به بازار جهانی معرفی نمود.
لوماکافتور(Lumacaftor): این دارو در جهت اصلاح مسیر انتقال پروتئین بیان شده توسط ژن کد کننده کانال غشایی انتقال دهنده کلر، از سیتوسل به سمت لایه خارجی غشاء پلاسمایی سلول عمل می کند. با استفاده از این دارو، شاهد افزایش حضور این پروتئین ها در اطراف غشاء پلاسمایی در سلول های افراد مبتلا به سیستیک فیبروزیس خواهیم بود.
ایواکافتور(Ivacaftor): این دارو در جهت باز نگه داشتن کانال غشایی انتقال دهنده کلر و افزایش عبور مواد از این کانال در غشاء پلاسمایی عمل می کند. با استفاده از این دو دارو، ما شاهد افزایش خروج یون کلراید از غشاء سلول و کاهش علائم این بیماران خواهیم بود.
شخصی سازی درمان بیماری سیتیک فیبروزیس:
شخصی سازی درمان شامل دو بخش می باشد. در بخش اول جهش های دخیل در کانال غشایی تنظیم کننده کلر (CFTR) از طریق بررسی های ژنتیکی مشخص می گردد. رایج ترین جهش F508 می باشد.
بخش دوم شامل مدل سازی ارگانوئیدی از بافت منشا گرفته از بیماران مبتلا به سیستیک فیبروزیس با جهش های دخیل در کانال غشایی تنظیم کننده کلر می باشد. پیشرفت در تکنولوژی مدل سازی ارگانوئیدی از بافت منشاء گرفته بیمار، این امکان را فراهم آورده است که بتوان با استفاده از نمونه بافت بیمار، درمان بیماران مبتلا به سیستیک فیبروزیس را شخصی سازی کرد. این مدل های برون تنی (In vitro)، به علت شباهت بسیار زیاد به لحاظ خصوصیات فیزیولوژیکی و ژنتیکی با بافت درون تنی بیمار (In vivo)، این قابلیت را فراهم آروده است که پاسخ دهی دارویی بر روی مدل های ارگانوئیدی بیمار، بطور دقیق منعکس کننده رفتار دارویی بر روی بافت بیمار باشد.